政策法規(guī) || 《罕見病用化學藥物藥學研究指導原則(征求意見稿)》(附法規(guī)概覽8.11-8.15)
01
關于公開征求《罕見病用化學藥物藥學研究指導原則(征求意見稿)》意見的通知

掃描圖中二維碼
查看詳細信息

01
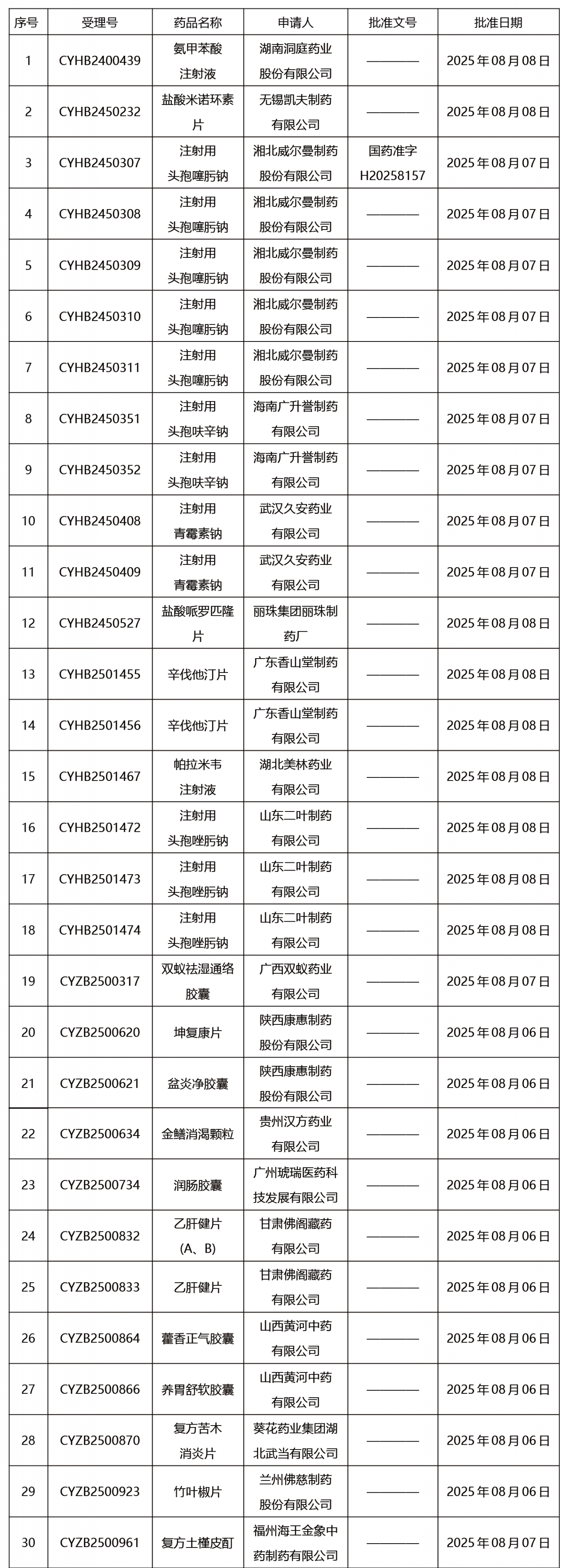
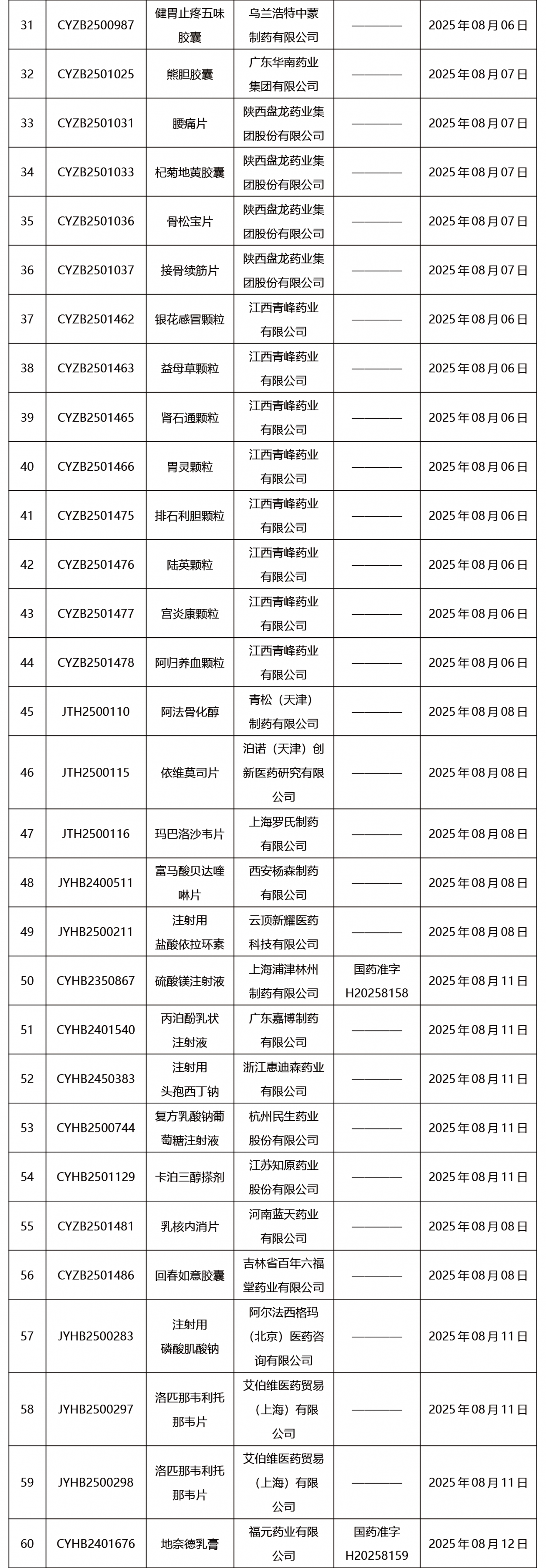
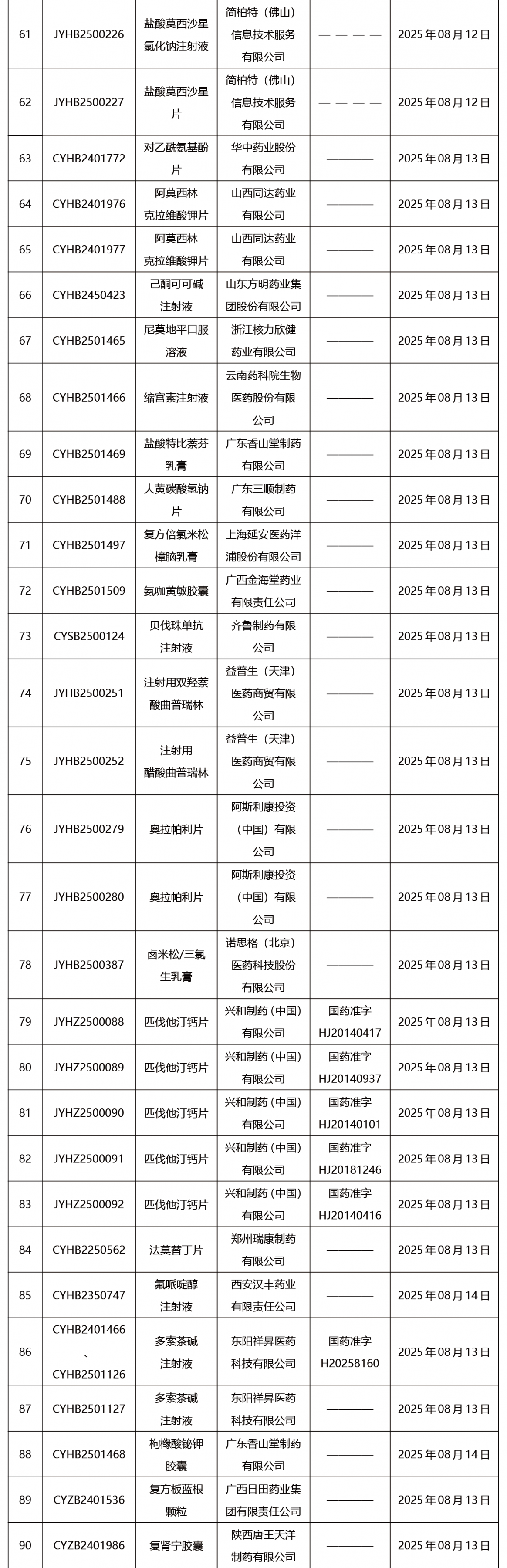
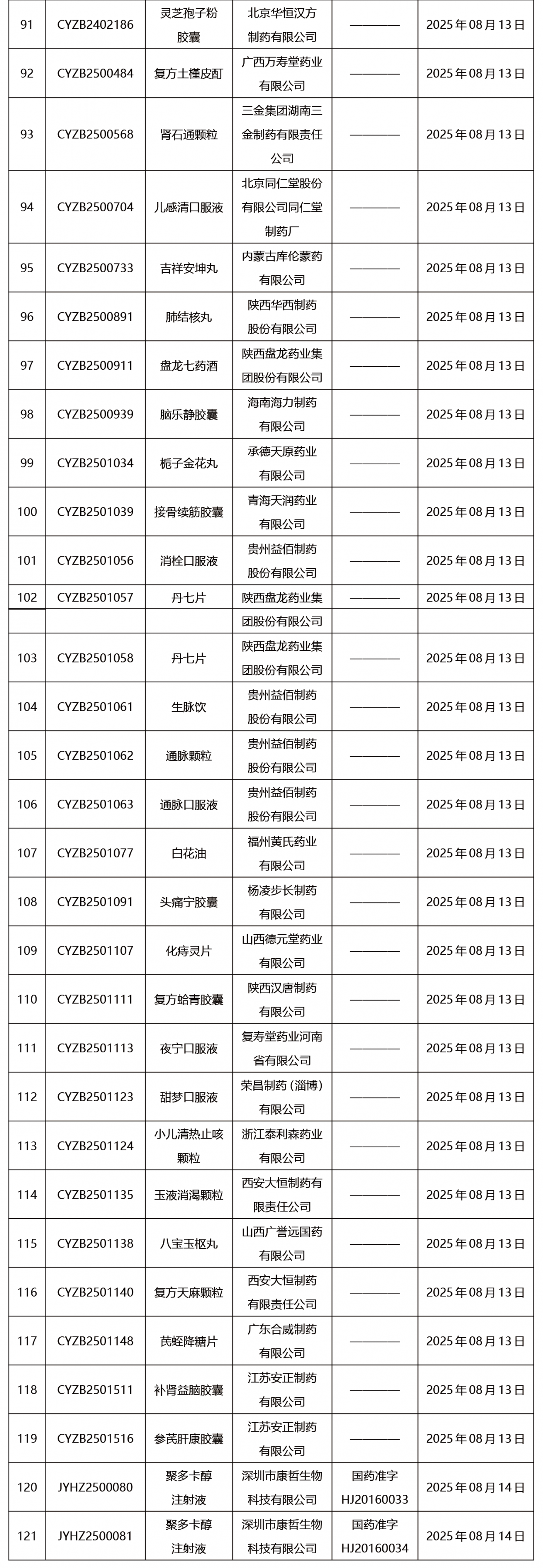
本周發(fā)布121項待領取藥品批準證明文件。
01
藥審中心舉辦2025年第七期“藥審云課堂”
掃描圖中二維碼
查看詳細信息

02
國家藥品監(jiān)督管理局藥品審評中心2024年度部門決算公開

掃描圖中二維碼
查看詳細信息

03
關于公開征求《藥物臨床試驗中應用貝葉斯外部信息借用方法的指導原則(征求意見稿)》意見的通知

掃描圖中二維碼
查看詳細信息

04
國家藥監(jiān)局藥審中心關于發(fā)布《骨關節(jié)炎新藥臨床研發(fā)技術(shù)指導原則》的通告(2025年第33號)

掃描圖中二維碼
查看詳細信息

05
關于公開征求ICH《M4Q(R2):人用藥品注冊通用技術(shù)文檔:質(zhì)量》指導原則草案意見的通知

掃描圖中二維碼
查看詳細信息

01
國家藥品監(jiān)督管理局特殊藥品檢查中心公開征求《放射性藥品生產(chǎn)檢查要點分解及 風險研判指導原則(征求意見稿)》意見
掃描圖中二維碼
查看詳細信息

02
國家藥品監(jiān)督管理局特殊藥品檢查中心公開征求《麻醉藥品精神藥品和藥品類易制毒化學品生產(chǎn)安全管理檢查要點分解及風險研判指導原則(征求意見稿)》意見
掃描圖中二維碼
查看詳細信息

-END-


轉(zhuǎn)載聲明:未經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán),不得轉(zhuǎn)載、摘編或利用其他方式使用上述作品。已經(jīng)本網(wǎng)或本網(wǎng)權(quán)利人授權(quán)使用作品的,應在授權(quán)范圍內(nèi)使用,并注明“來源:新領先醫(yī)藥科技”。

 Hotline服務熱線:010-83057670
Hotline服務熱線:010-83057670
 簡體中文
簡體中文

 010-83057670
010-83057670 聯(lián)系地址:
聯(lián)系地址: 技術(shù)市場部:
技術(shù)市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
